速遞 優瑞科生物兩款T細胞療法獲FDA孤兒藥資格,引領肝細胞癌治療新紀元
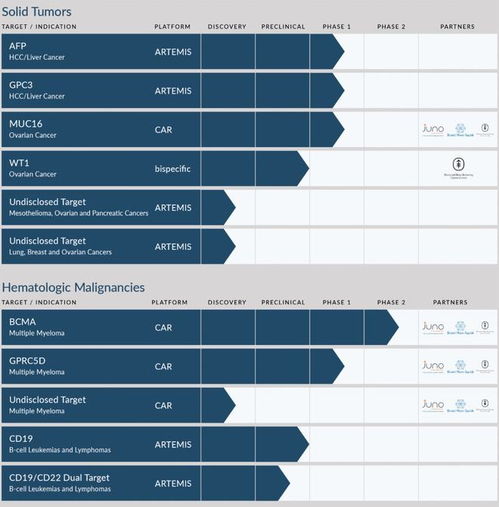
生物醫藥領域傳來重要進展。優瑞科生物(Eurica)宣布,其針對肝細胞癌(HCC)開發的兩款創新型T細胞療法,已獲得美國食品藥品監督管理局(FDA)授予的孤兒藥資格。這一資格認定,不僅是對這兩款療法在治療這一難治性癌癥方面潛力的重要認可,也標志著細胞免疫療法在實體瘤治療領域的應用取得了新的突破。
肝細胞癌是最常見的原發性肝癌,在全球范圍內發病率和死亡率均居高不下,尤其在中國等亞洲國家負擔沉重。目前,對于晚期或不可切除的肝細胞癌,盡管有靶向治療和免疫檢查點抑制劑等方案,但患者總體預后仍然不佳,存在巨大的未滿足臨床需求。T細胞療法,特別是經過基因工程改造的T細胞療法,通過增強患者自身免疫系統識別和攻擊癌細胞的能力,為攻克實體瘤帶來了全新的希望。
據悉,優瑞科生物此次獲得孤兒藥資格的兩款療法,均基于其獨特的T細胞工程化平臺。它們旨在通過不同的作用機制,精準靶向肝細胞癌腫瘤細胞表面的特定抗原,從而實現對癌細胞的定向清除,同時盡可能減少對正常組織的損傷。FDA的孤兒藥資格旨在鼓勵和促進用于治療罕見病(在美國患者人數少于20萬的疾病)的藥物或生物制品的開發。獲得該資格的藥物,在研發過程中可獲得一系列政策支持,包括臨床試驗費用的稅收抵免、免除新藥申請費,以及藥品獲批后享有七年的市場獨占期。這不僅將顯著降低優瑞科生物的研發成本與風險,也將加速這兩款療法后續的臨床試驗進程和最終的上市步伐。
從更廣闊的網絡工程視角來看,此次進展也是生物醫藥研發“網絡”中一個關鍵節點的成功激活。現代新藥研發,尤其是前沿的細胞與基因療法,高度依賴于一個復雜而協同的“網絡工程”體系。這個體系包括:基礎研究的發現網絡(如對肝癌新抗原的識別)、技術開發平臺網絡(如基因編輯與病毒載體技術)、臨床試驗執行網絡(多中心協作)、法規審批協同網絡(與FDA等機構的溝通),以及資本與產業鏈的支持網絡。優瑞科生物的成果,正是其內部研發“網絡”高效運作,并與外部產業、監管、資本“網絡”成功對接的體現。它像是一個精心設計和調試的生物“程序”,在龐大的醫藥生態“系統”中成功運行并獲得了階段性“輸出”認證。
隨著這兩款療法后續臨床研究的深入,它們有望為肝細胞癌患者提供更有效、更個性化的治療選擇。這一進展也將進一步激勵全球生物科技公司加大對實體瘤細胞療法的投入,推動整個腫瘤治療“網絡”的升級與迭代。挑戰依然存在,包括如何進一步提高療法在實體瘤中的浸潤效率、克服腫瘤微環境的免疫抑制以及控制潛在副作用等。但毋庸置疑,優瑞科生物此次獲得的孤兒藥資格,無疑為肝細胞癌的治療賽道點亮了一盞新的指路明燈,也為通過前沿生物技術“網絡工程”攻克重大疾病樹立了又一個里程碑。
如若轉載,請注明出處:http://m.wfqite.com/product/65.html
更新時間:2026-02-24 02:37:20